Diagrama ferro-carbono. O diagrama do estado do sistema ferro-carbono
É difícil imaginar uma construção modernamáquinas, máquinas e outras indústrias importantes sem o uso das principais ligas metálicas de aço e ferro fundido. Sua produção excede todas as outras em dezenas de vezes.
Se considerarmos aço e ferro fundido em termos detais como ciência metalúrgica, a figura central aparece diagrama de fase ferro-carbono, que proporciona uma apresentação detalhada sobre a estrutura e as transformações estruturais nestes materiais. E também para atender a sua composição de fase.

História da descoberta
A primeira vez que em ligas (aços e ferros fundidos)há certos pontos (especiais), apontou o grande metalurgista e inventor - Dmitry Konstantinovich Chernov (1868). Foi ele quem fez uma descoberta importante sobre as transformações polimórficas e é um dos criadores do diagrama do estado do ferro-carbono. Segundo Chernov, a posição desses pontos no diagrama depende diretamente da porcentagem de carbono.
E o que é mais interessante, é a partir do momento da descoberta que a ciência como a metalografia começa a sua vida.
O diagrama de ligas de ferro com carbono é o resultado do trabalho meticuloso de cientistas de vários países do mundo. Todas as designações alfabéticas dos principais pontos e fases no diagrama são internacionais.
O conceito de um diagrama
Representação gráfica dos processos que ocorrem emliga com uma mudança no regime de temperatura, a concentração de substâncias, a pressão, é chamado o diagrama de estado. Ele permite que você visualize visualmente e visualmente todas as transformações que ocorrem nas ligas.
Elementos do diagrama ferro-carbono
Breve informação sobre cada um destes elementos.
O ferro é um metal cinza prateado. Gravidade específica - 7, 86 g / cm3. Tem um ponto de fusão de 1539 ° C.
A interação de ferro e outros metais produz compostos chamados soluções de substituição. Se com não-metais, por exemplo, com carbono ou hidrogênio, então - com soluções de implantação.
O ferro tem a capacidade de ser originalmentesólido, estar em vários estados, que são chamados de "alfa" e "gama" em metalurgia. Essa qualidade é chamada de polimorfismo. Sobre isso mais adiante no artigo.
Carbono não é metal. Se atua como grafite, então o ponto de fusão é 3500 ° C. Se é como um diamante, é 5000 ° C. A densidade do carbono é de 2,5 g / cm3. Também possui propriedades polimórficas.
Em ligas de ferro-carbono, este elemento forma uma solução sólida, que contém um ferrum, chamado cementita (Fe3C) Forma também grafite em ferro fundido.
Diagrama de liga de ferro-carbono
Em consequência da interação dos componentes do diagrama um com outro, resulta cementite - um composto químico.
Como regra, ao estudar um diagrama por estudantes de metal, todos os compostos estáveis são considerados como componentes, e a própria imagem gráfica é examinada em partes.
Também na sala de aula, uma curva de resfriamento é construída de acordo com o diagrama ferro-carbono: a porcentagem de carbono é selecionada e, em seguida, é necessário determinar qual fase corresponde a qual temperatura no diagrama.
Para fazer isso, além do próprio diagramadesenhe um sistema de coordenadas (temperatura-tempo). E partindo dos graus máximos, mova-se gradualmente para baixo, representando a curva e as áreas de transição de uma fase para outra. É necessário chamá-los e indicar o tipo de rede cristalina.
Em seguida, consideramos mais detalhadamente a imagem gráfica do diagrama de estado do ferro-carbono.
Primeiro, tem duas formas (partes):
- cementita de ferro;
- grafite de ferro.
Em segundo lugar, as ligas, nas quais os principais "atores" são ferrum e carbono, são convencionalmente divididos em:
- aço;
- ferro fundido
Se o carbono na liga é menor ou igual a 2,14% (ponto E no diagrama), então é de aço, se mais de 2,14%, é de ferro fundido. Por esse motivo, o diagrama é dividido em duas fases.
Transformações polimórficas
Mais detalhes sobre cada fase abaixo no artigo. Em suma, a implementação das principais transformações ocorre em temperaturas especiais.
O estado do ferro é designado por α-ferrum (a uma temperatura inferior a 911 ° C). A rede cristalina é um cubo volumétrico centralizado na face. Ou cco. A distância entre os átomos de tal rede é bastante alta.
O ferro adquire uma modificação gama, isto é, é designado como γ-ferrum (911-1392 ° C). A estrutura cristalina é um cubo centrado na face (fcc). Nesta rede, a distância entre os átomos é menor que na cúbica.
Na transição α-ferrum em γ-ferrum o volume de matériaficando menor. A razão para isso é a treliça de cristal - sua aparência. Porque a rede fc tem um estado de átomos mais ordenado que o bcc.
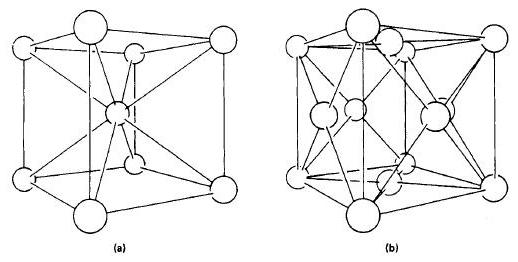
Se a transição é realizada na direção oposta - de γ-ferrum para α-ferrum, então o volume da liga aumenta.
Quando a temperatura atinge 1392 ° C (masinferior ao ponto de fusão do ferro a 1539 ° C), então o α-ferrum se transforma em um δ-ferrum, mas essa não é sua nova forma, mas apenas uma variedade. Além disso, o δ-ferrum é uma estrutura instável.
Propriedades de ferro tecnicamente puro
Propriedades magnéticas do ferro a várias temperaturas:
- inferior a 768 ° C - ferromagnético;
- mais de 768 ° С - paramagnetic.
Um ponto de temperatura de 768 ° C é chamado de ponto de transformação magnética, ou o ponto de Curie.
Propriedades do ferro tecnicamente puro:
- dureza - 80 HB;
- resistência temporária - 250 MPa;
- limite de elasticidade - 120 MPa;
- alongamento relativo de 50%;
- estreitamento relativo - 80%;
- alto módulo de elasticidade.

Carboneto de ferro
Vista gráfica da parte componente do diagrama ferro-carbono: Fe3C. A substância é chamada de carboneto de ferro ou cementita. É típico para ele:
- Teor de carbono de 6,67%.
- Peso específico - 7,82%.
- A rede cristalina tem uma forma rômbica, consistindo de octaedro.
- A fusão ocorre a uma temperatura de 601260 ° C.
- Baixas propriedades ferromagnéticas a baixas temperaturas.
- Dureza - 800 HB.
- A plasticidade é quase zero.
- O carboneto de ferro forma soluções sólidas.substituições nas quais átomos de carbono são substituídos por átomos não-metálicos (nitrogênio) e átomos de ferro - por metais (cromo, tungstênio, manganês). Esta composição sólida é chamada de liga.
Como mencionado acima, a cementita éfase instável e grafite - estável. Desde que a primeira substância é um composto instável, desintegrando-se sob certas condições de temperatura.

No diagrama ferro-carbono existem tais estados:
- fase líquida;
- ferrite;
- austenite;
- cementite;
- grafite;
- perlita;
- ledeburit.
Considere cada um deles em detalhes.
Fase líquida
O ferrum no estado líquido dissolve bem o carbono. Isto é, independentemente de qual proporção eles estão em porcentagem de conteúdo. O resultado é uma massa líquida homogênea.

Ferrite
É uma solução sólida introduzindo carbono emα-ferrum. Uma pequena quantidade de impurezas também pode ser incluída. Mas a ferrita tem quase a mesma qualidade que o ferro puro. Se examinarmos a estrutura sob um microscópio, podemos ver grãos poliédricos de tom claro.
Acontece:
- baixa temperatura (a uma temperatura de 727 ° C, a solubilidade do carbono é de 0,02%);
- alta temperatura (a 1499 ° C, a solubilidade do carbono é de 0,1%), ou é chamado δ-ferrum.
Propriedades da ferrita:
- dureza - 80-120 HB;
- resistência temporária - 300 MPa;
- alongamento relativo - 50%;
- tem boas propriedades magnéticas (até uma temperatura de 768 ° C).
Austenita
Esta é uma solução sólida que introduz o carbonoγ-ferrum. Também pode estar em uma pequena quantidade de impureza. Na estrutura cristalina, o carbono está no centro da célula da Fcc. Ao examinar a estrutura da austenita sob um microscópio, ela é visível como grãos leves de forma poliédrica com gêmeos.
Tem as seguintes características:
- A solubilidade do carbono no γ-ferrum é de 2,14% (a uma temperatura de 1147º С).
- 180 dureza de austenita;
- Alongamento - 40-50%;
- Boa qualidade paramagnética.
Cimento e suas formas
Presente nas seguintes fases: C1, C2, C3 (cementita primária, secundária e terciária).
Quanto aos indicadores físico-químicos desses três estados, eles são aproximadamente iguais. As propriedades mecânicas são afetadas pelo tamanho das partículas, seu número e localização.
Você também pode ver no diagrama que:
- C1 é formado a partir de um estado líquido (sob um microscópio, é visível como uma placa de tamanho grande);
- C2 - de austenita (localizada em torno de seus grãos na forma de uma grade);
- C3 - a partir de ferrita (localizada nas bordas dos grãos ferríticos na forma de pequenas partículas).
Perlite e Ledeburite
Uma mistura de ferrita e cementita é chamada de perlita. É formado durante a decomposição de austenite (a uma temperatura inferior a 727 ° C). Quando ampliada, essa estrutura está na forma de placas ou grãos.
A perlita com diminuição gradual da temperatura está presente em todas as ligas com um teor de carbono de 0,02 a 6,67%.
Ledeburite - uma mistura de austenita e cementita. É formado a partir da fase líquida quando resfriado a uma temperatura abaixo de 1147 ° C.
Ferro fundido
Ligas no diagrama de ferro-carbono quecontêm carbono mais que 2.14%, chamado ferro fundido. Eles são altamente frágeis. A seção transversal de tal ferro fundido tem um tom claro e, portanto, é chamado de ferro fundido branco.
No diagrama, este é o ponto C, chamado eutético,com um conteúdo de carbono correspondente de 4,3%. Quando a cristalização forma uma mistura consistindo de austenita e cementita, coletivamente denominada ledeburit. A composição da fase é constante.
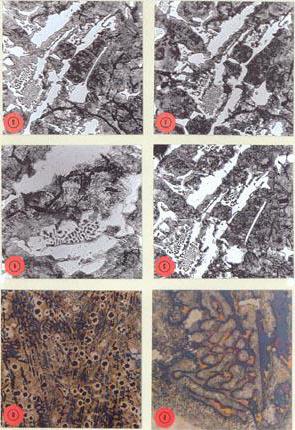
Quando a concentração de carbono é inferior a 4,3%(ferro fundido hipoeutético) durante a cristalização, a austenita é liberada da solução. Além disso, de lá se destaca C2. E a 727 ° C, a austenita se transforma em perlita. O estado estrutural de tal ferro fundido é o seguinte: grandes porções de perlita de tom escuro.
Em ferro fundido branco hipereutético (carbono mais4,3%) após o resfriamento, a estruturação ocorre com a formação de cristais C1. Outras transformações são realizadas já no estado sólido. A estrutura é um ledeburite, que é o fundo para campos de perlita de cor escura. E grandes estratos são C1.

Conclusões
Alcançar o equilíbrio absoluto, físico e químico, é impossível, exceto em condições especiais de laboratório.
Na prática, o equilíbrio pode ser aproximado paraabsoluto, mas sob certas condições: aumentar ou diminuir lentamente a temperatura da liga, que será mantida por um longo tempo.





